Разработка и валидация количественного ВЭЖХ-МС/МС метода определения пиперациллина в плазме крови
DOI:
https://doi.org/10.18413/rrpharmacology.9.10027Аннотация
Введение: Снижение смертности пациентов с сепсисом, принимающие пиперациллин, возможно при получении ими длительной инфузии, что улучшает воздействие противомикробных препаратов. Однако такая терапия пиперациллином требует проведения терапевтического лекарственного мониторинга, применение новейшего аналитического оборудования и разработанных методик количественного определения пиперациллина.
Материалы и методы: Для приготовления маточных и стандартных растворов пипирецилинаиспользовались сухие навески соответствующих сертифицированных стандартов пипирецилина. Разделение компонентов проводили с использованием ВЭЖХ системы Agilent 1260 с бинарным насосом и термостатируемым автосемплером. Анализируемые вещества детектировали с помощью гибридной масс-спектрометрической системы Sciex QTRAP 5500. Валидация разработанного метода проводилась в соответствии с правилами проведения исследований биоэквивалентности лекарственных препаратов в рамках Евразийского экономического союза; 2016. – Астана.
Результаты и их обсуждения: Ионы-«предшественники» пиперациллина соответствовали частицам m/z 518,2. Наиболее интенсивными ионами-«продуктами», зарегистрированными при фрагментации протонированных молекул в ячейке соударений, были частицы m/z 143,1, m/z 115,0. При валидации разработанного метода были установлены основные валидационные параметры: линейность, точность, правильность, чувствительность (нижний предел количественного определения).
Заключение: Подтвержденный аналитический диапазон методики составил 0,5–100 мкг/мл в плазме крови. Полученный аналитический диапазон позволяет применять разработанную методику для проведения аналитической части исследований фармакокинетики пиперацилина.
Графическая аннотация
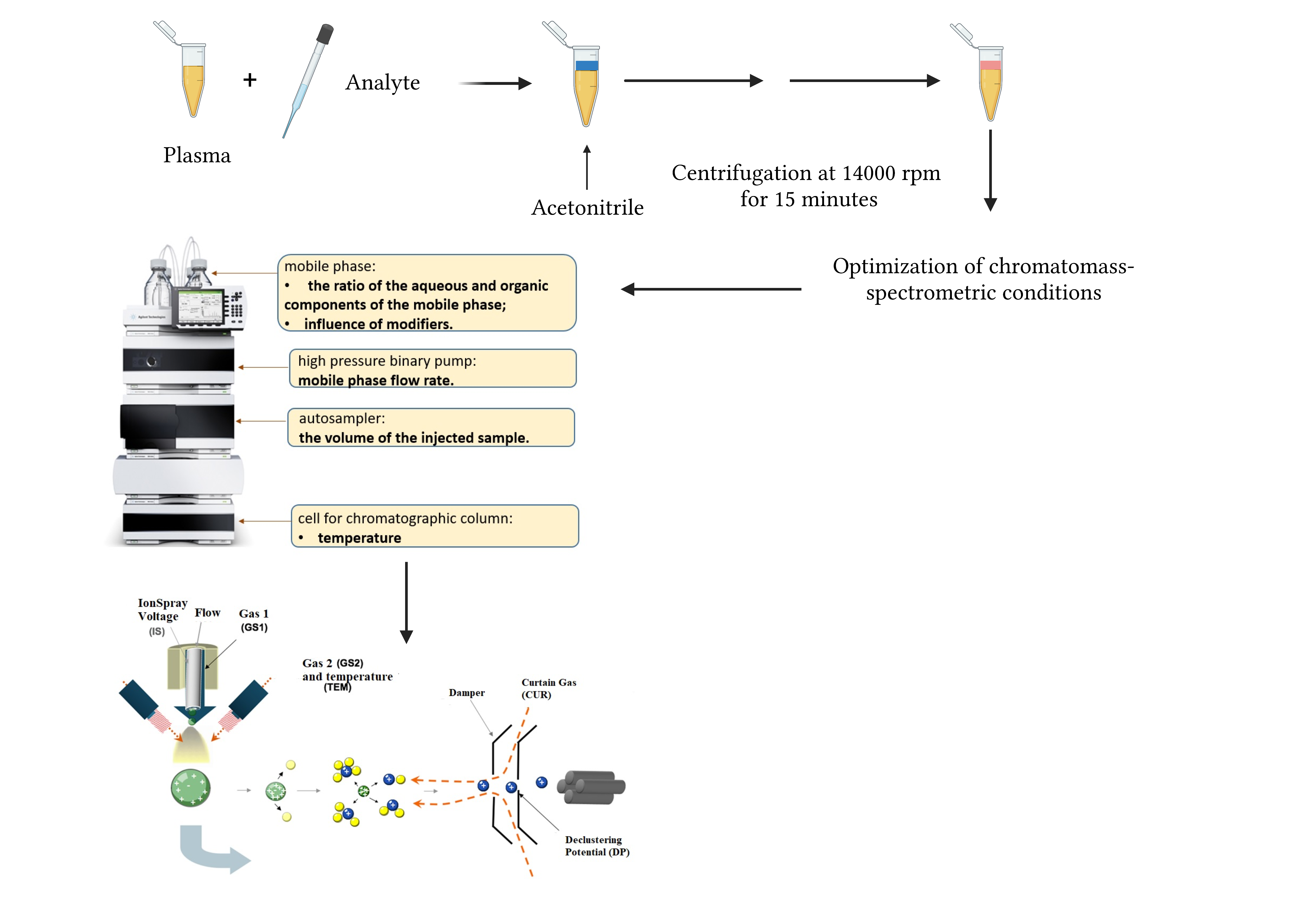
Ключевые слова:
ВЭЖХ/МС, валидация, количественный анализ, пиперациллин, биоаналитикаБиблиографические ссылки
Anikeev IS, Osadchenko NA, Basargina PS, Zhukovskaya YuA, Mileeva YuS (2018) Development of a highly sensitive chromato-mass spectrometric method for the determination of vancomycin and piperacillin in blood plasma. In: Actual Problems of Experimental and Clinical Medicine Materials of the 76th international scientific and practical conference of young scientists and students, VolgGMU, Volgograd p. 521–522. [in Russian]
Council of the Eurasian Economic Commission (2016) On approval of the rules for conducting bioequivalence studies of medicinal products within the framework of the Eurasian Economic Union, Astana, 161 pp. [in Russian]
Barco S, Bandettini R, Maffia A, Tripodi G, Castagnola E, Cangemi G (2015) Quantification of piperacillin, tazobactam, meropenem, ceftazidime, and linezolid in human plasma by liquid chromatography/tandem mass spectrometry. Journal of Chemotherapy 27(6): 343–347. https://doi.org/10.1179/1973947814Y.0000000209 [PubMed]
Berm EJ, Odigie B, Bijlsma MJ, Wilffert B, Touw DJ, Maring JG (2016) A clinical validation study for application of DBS in therapeutic drug monitoring of antidepressants. Bioanalysis 8(5): 413–424. https://doi.org/10.4155/bio.15.255[PubMed]
Capiau S, Veenhof H, Koster RA, Bergqvist Y, Boettcher M, Halmingh O, Keevil BG, Koch BCP, Linden R, Pistos C, Stolk LM, Touw DJ, Stove CP, Alffenaar JC (2019) Official International association for therapeutic drug monitoring and clinical toxicology guideline: Development and validation of dried blood spot-based methods for therapeutic drug monitoring. Therapeutic Drug Monitoring 41(4): 409–430. https://doi.org/10.1097/FTD.0000000000000643 [PubMed]
Cohen-Wolkowiez M, Watt KM, Zhou C, Bloom BT, Poindexter B, Castro L, Gao J, Capparelli EV, Benjamin DK Jr, Smith PB. (2014) Developmental pharmacokinetics of piperacillin and tazobactam using plasma and dried blood spots from infants. Antimicrobial Agents and Chemotherapy 58(5): 2856–2865. https://doi.org/10.1128/AAC.02139-13[PubMed] [PMC]
D'Cunha R. et al. Quantification of cefepime, meropenem, piperacillin and tazobactam in human plasma using a sensitive and robust LC-MS/MS method-Part I. Assay development and validation //Antimicrobial Agents and Chemotherapy. – 2018. – С. AAC. 00859-18. https://doi.org/10.1128/AAC.00859-18 [PubMed] [PMC]
Fan Y, Peng X, Yu J, Liang X, Chen Y, Liu X, Guo B, Zhang J (2019) An ultra-performance liquid chromatography-tandem mass spectrometry method to quantify vancomycin in human serum by minimizing the degradation product and matrix interference. Bioanalysis 11(10): 941–955. https://doi.org/10.4155/bio-2018-0310 [PubMed]
Hagel S, Fiedler S, Hohn A, Brinkmann A, Frey OR, Hoyer H, Schlattmann P, Kiehntopf M, Roberts JA, Pletz MW; TARGET Study Group (2019) Therapeutic drug monitoring-based dose optimization of piperacillin/tazobactam to improve outcome in patients with sepsis (TARGET): a prospective, multi-centre, randomised controlled trial. Trials 20(1): 330. https://doi.org/10.1186/s13063-019-3437-x [PubMed] [PMC]
Jager NG, Rosing H, Schellens JH, Beijnen JH (2014) Procedures and practices for the validation of bioanalytical methods using dried blood spots: a review. Bioanalysis 6(18): 2481–2514. https://doi.org/10.4155/bio.14.185 [PubMed]
Keçeli SA, Willke A, Tamer GS, Boral OB, Sonmez N, Cağatay P (2014) Interaction between caspofungin or voriconazole and cefoperazone-sulbactam or piperacillin-tazobactam by in vitro and in vivo methods. APMIS 122(5): 412–417. https://doi.org/10.1111/apm.12159 [PubMed]
Li Z, Li Q, Wang Y, Cao D, Chen C (2012) Determination of free and total piperacillin–tazobactam in plasma by HPLC–MS–MS: An adapted method for neonates. Chromatographia 75: 533–539 https://doi.org/10.1007/s10337-012-2214-8
Li Q, Cao D, Huang Y, Xu H, Yu C, Li Z (2013) Development and validation of a sensitive LC-MS/MS method for determination of tacrolimus on dried blood spots. Biomedical Chromatography 27(3): 327–334. https://doi.org/10.1002/bmc.2795
Mu A (2019) The application of dried blood spots in toxicokinetic and pharmacokinetic studies. Journal of Chemical Information and Modeling 9: 1689–1699.
Schmitt V, Szeitz A, Klassen T, Häfeli U (2017) An ultra-high performance liquid chromatography-tandem mass spectrometry method for the quantification of vancomycin requiring only 2 µL of rabbit serum. American Journal of Analytical Chemistry 8(9): 553–563. https://doi.org/10.4236/ajac.2017.89040
Timmerman P, White S, Globig S, Lüdtke S, Brunet L, Smeraglia J (2011) EBF recommendation on the validation of bioanalytical methods for dried blood spots. Bioanalysis 3(14): 1567–1575. https://doi.org/10.4155/bio.11.132 [PubMed]
Verhoven SM, Groszek JJ, Fissell WH, Seegmiller A, Colby J, Patel P, Verstraete A, Shotwell M (2018) Therapeutic drug monitoring of piperacillin and tazobactam by RP-HPLC of residual blood specimens. Clinica Chimica Acta 482: 60–65. https://doi.org/10.1016/j.cca.2018.03.021 [PubMed] [PMC]
 Русский
Русский
 English
English

