Ингибитор α-амилазы акарбоза эффективен при длительном применении в отношении симптомов развития сахарного диабета 2 типа у мышей C57BL/6
DOI:
https://doi.org/10.18413/rrpharmacology.10.455Аннотация
Введение. Важным классом антигипергликемических препаратов второй линии являются ингибиторы α-амилаз, действие которых заключается в замедлении расщепления и всасывания углеводов, что снижает пиковую концентрацию глюкозы при приеме пищи. Однако в последнее время сообщается о других благоприятных эффектах приема ингибиторов α-амилаз на фоне сахарного диабета 2 типа (СД2).
Материалы и методы. Моделирование СД2 проводилось путем содержания мышей C57BL/6 на высокожировой диете в течение 21 недели. Начиная с 18 недели, животным в течение 4 недель перорально вводилась акарбоза в дозе 24 мг/кг или препарат сравнения метформин в дозе 200 мг/кг. В период введения тестируемых веществ отслеживались прирост массы тела, масса висцерального жира и диаметр адипоцитов, а также проводились глюкозотолерантный крахмальный тест, инсулинорезистентный тест и измерялась концентрация глюкозы натощак.
Результаты. Введение акарбозы в течение 2 и 4 недель привело к значительному снижению постпрандиального уровня глюкозы при проведении крахмального теста, AUC под графиком концентрации глюкозы была значительно ниже после введения акарбозы в дозе 24 мг/кг на фоне моделирования СД2. Акарбоза в дозе 24 мг/кг эффективно снижала уровень глюкозы натощак через 2 и 4 недели ежедневного перорального введения наравне с метформином. Введение акарбозы в дозе 24 мг/кг в течение 2 и 4 недель привело к значительному снижению AUC концентрации глюкозы в инсулинорезистентном тесте. Акарбоза способствовала значительному снижению диаметра адипоцитов, и прироста массы тела на фоне моделирования СД2.
Выводы. Акарбоза в дозе 24 мг/кг проявляет эффективность не только в снижении постпрандиального уровня глюкозы на фоне СД2, что вызвано ее ингибиторной активностью α-амилаз, но и облегчает инсулинорезистентность, снижает базальную концентрацию глюкозы и предотвращает развитие ожирения, что может быть связано со стимулированием секреции GLP-1.
Графическая аннотация
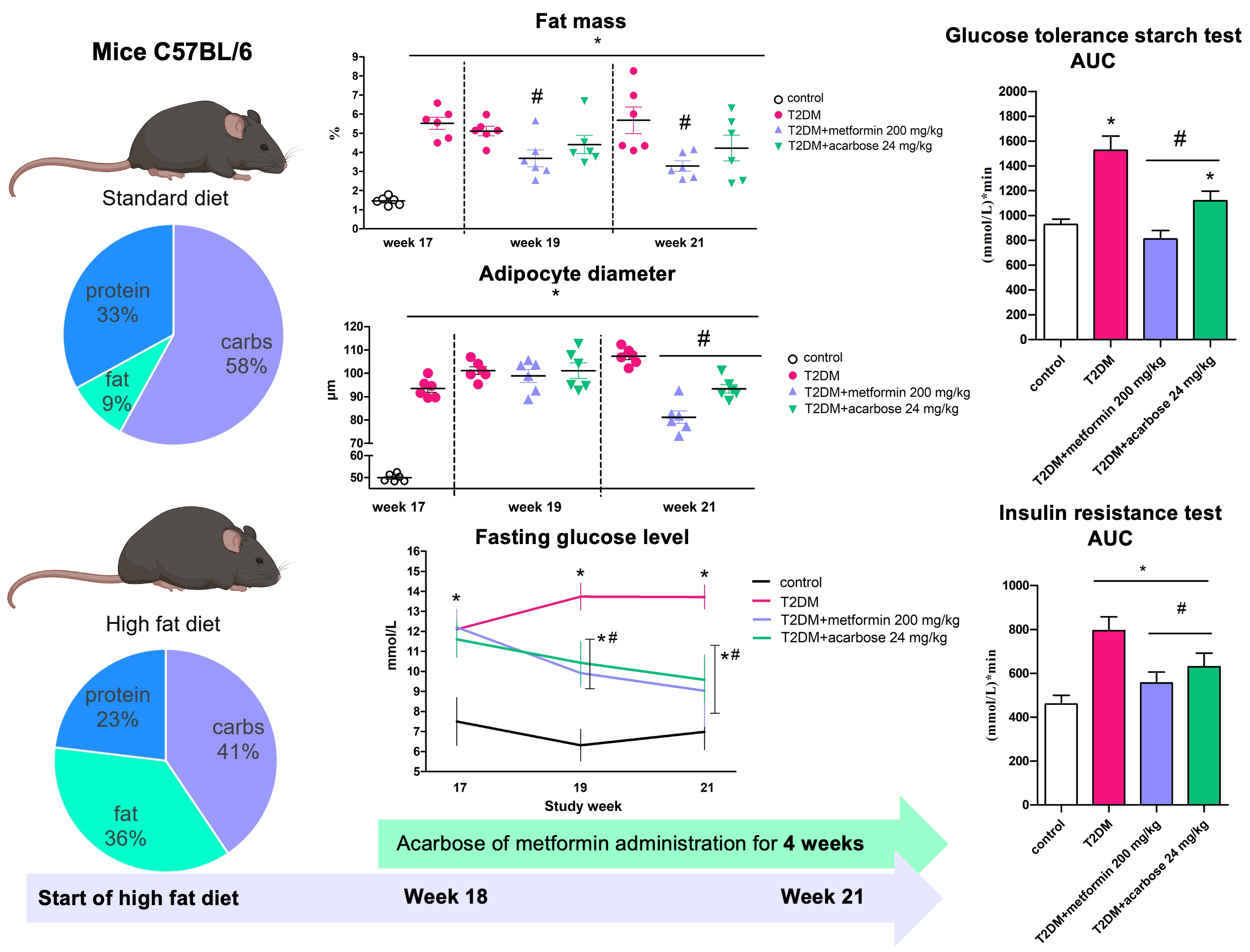
Ключевые слова:
акарбоза, ингибиторы α-амилаз, инсулинорезистентность, сахарный диабет 2 типа, мыши C57BL/6Библиографические ссылки
Altay M (2022) Acarbose is again on the stage. World Journal of Diabetes 13(1): 1–4. https://doi.org/10.4239/wjd.v13.i1.1
Borozdina NA, Shaikhutdinova ER, Slashcheva GA, Goryacheva NA, Zamyatina AV, Sadovnikova ES, Pakhomova IA, Pavlov VM, Perepechenova NA, Severyukhina MS, Fedotova AY, Popkova DV, Gladkikh IN, Leichenko EV, Dyachenko IA (2023) Characterization of risk factors for modeling of a type 2 diabetes mellitus induced by a high-fat diet in C57BL/6 mice. Bulletin of Experimental Biology and Medicine [Byulleten’ Eksperimental’noi Biologhii i Meditsiny] 176(10): 460–464. https://doi.org/10.47056/0365-9615-2023-176-10-460-464 [in Russian]
Dalsgaard NB, Gasbjerg LS, Hansen LS, Hansen NL, Stensen S, Hartmann B, Rehfeld JF, Holst JJ, Vilsbøll T, Knop FK (2021) The role of GLP-1 in the postprandial effects of acarbose in type 2 diabetes. European Journal of Endocrinology 184(3): 383–394.https://doi.org/10.1530/EJE-20-1121
Gerstein HC, Coleman RL, Scott CAB, Xu S, Tuomilehto J, Rydén L, Holman RR (2020) ACE Study Group. Impact of acarbose on incident diabetes and regression to normoglycemia in people with coronary heart disease and impaired glucose tolerance: Insights from the ACE Trial. Diabetes Care 43(9): 2242–2247. https://doi.org/10.2337/dc19-2057
Krasilnikova EI, Blagosklonnaya YV, Baranova EI, Grineva EN, Bystrova AA, Ryumina IA, Volkova AR, Karonova TL (2023) The role of acarbose in the treatment and prevention of diabetes mellitus type 2: New opportunities in cardiovascular risk decrease. Arterial Hypertension [Arterial’naya Ghipertenziya] 15(6): 640–647. https://doi.org/10.18705/1607-419X-2009-15-6-640-647 [in Russian]
Lee JO, Lee SK, Kim JH, Kim N, You GY, Moon JW, Kim SJ, Park SH, Kim HS (2012) Metformin regulates glucose transporter 4 (GLUT4) translocation through AMP-activated protein kinase (AMPK)-mediated Cbl/CAP signaling in 3T3-L1 preadipocyte cells. Journal of Biological Chemistry 287(53): 44121–4412https://doi.org/10.1074/jbc.m113.492017
Li Y, Zhang W, Zhao R, Zhang X (2022) Advances in oral peptide drug nanoparticles for diabetes mellitus treatment. Bioactive Materials 15: 392–408. https://doi.org/10.1016/j.bioactmat.2022.02.025
Petersons CJ (2018). Second steps in managing type 2 diabetes. Australian Prescriber 41(5): 141–144. https://doi.org/10.18773/austprescr.2018.043
Rosak C, Mertes G (2012) Critical evaluation of the role of acarbose in the treatment of diabetes: patient considerations. Diabetes, Metabolic Syndrome and Obesity 5: 357–367. https://doi.org/10.2147/DMSO.S28340
Shestakova EA (2017) Second line therapy in type 2 diabetes: legacy effect activation. Diabetes Mellitus [Sakharnyi Diabet] 20(5): 356–362. https://doi.org/10.14341/DM8793[in Russian]
Song LL, Wang X, Yang ZJ, Kong XM, Chen XP, Zhang B, Yang WY (2020) Factors associated with improvement in waist-to-height ratio among newly diagnosed type 2 diabetes patients treated with acarbose or metformin: A randomized clinical trial study. World Journal of Diabetes 11(11): 514–526. https://doi.org/10.4239/wjd.v11.i11.514
Taslimi P, Aslan HE, Demir Y, Oztaskin N, Maraş A, Gulçin İ, Beydemir S, Goksu S (2018) Diarylmethanon, bromophenol and diarylmethane compounds: Discovery of potent aldose reductase, α-amylase and α-glycosidase inhibitors as new therapeutic approach in diabetes and functional hyperglycemia. International Journal of Biological Macromolecules 119: 857–863. https://doi.org/10.1016/j.ijbiomac.2018.08.008
Tomic D, Shaw JE, Magliano DJ (2022) The burden and risks of emerging complications of diabetes mellitus. Nature Reviews Endocrinology 18(9): 525–539. https://doi.org/10.1038/s41574-022-00690-7
Wong TY, Liew G, Tapp RJ, Schmidt MI, Wang JJ, Mitchell P, Klein R, Klein BE, Zimmet P, Shaw J (2008) Relation between fasting glucose and retinopathy for diagnosis of diabetes: three population-based cross-sectional studies. Lancet 371(9614): 736–43. https://doi.org/10.1016/S0140-6736(08)60343-8
Zamanian MY, Giménez-Llort L, Nikbakhtzadeh M, Kamiab Z, Heidari M, Bazmandegan G (2023) The therapeutic activities of metformin: focus on the Nrf2 signaling pathway and oxidative stress amelioration. Current Molecular Pharmacology 16(3): 331–345. https://doi.org/10.2174/1874467215666220620143655
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2024 Natalya A. Borozdin, Ekaterina N. Kazakova, Irina N. Gladkikh, Elena V. Leychenko, Igor A. Dyachenko

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

