Противотревожные свойства новых производных 5H-2,3-бензодиазепина и 5H-[1,2,5]триазепина
DOI:
https://doi.org/10.18413/rrpharmacology.11.808Аннотация
Введение. Поскольку полициклические производные диазепина и триазепина представляют интерес для изучения их психотропных свойств, в рамках предшествующих исследований изучены анксиолитические свойства соединений, сочетающих 5H-2,3-бензодиазепин и [1,2,4]триазол, а именно производных 7H-[1,2,4]триазоло[3,4-a][2,3]бензодиазепина. В рамках настоящей работы исследована другая группа производных 5H-2,3-бензодиазепина и 5H-[1,2,5]триазепина на предмет наличия психотропной активности.
Материалы и методы. На первом этапе исследования проводили оценку возможных видов психотропной активности и механизмов ее реализации среди указанных производных in silico с помощью тест-системы PASSonline. Поскольку, согласно прогнозу, для соединений характерна анксиолитическая активность, на втором этапе проводили скрининг указанных соединений in vivo в условиях теста «Приподнятый крестообразный лабиринт». На третьем этапе наблюдали влияние субстанций на поведение грызунов в тесте «Открытое поле», а также оценивали миорелаксирующий потенциал, характерный для диазепиновых производных, в тесте «Ротарод». На четвертом этапе анализировали взаимосвязь структурно-функциональных отношений среди изученных веществ. На последнем этапе некоторые свойства наиболее активных субстанций были оценены с помощью ADMET-анализа. В результате исследования были определены соединения с анксиолитическим действием, выделены фармакофоры, ответственные за проявление эффекта, а также предварительно оценена их безопасность для дальнейших исследований.
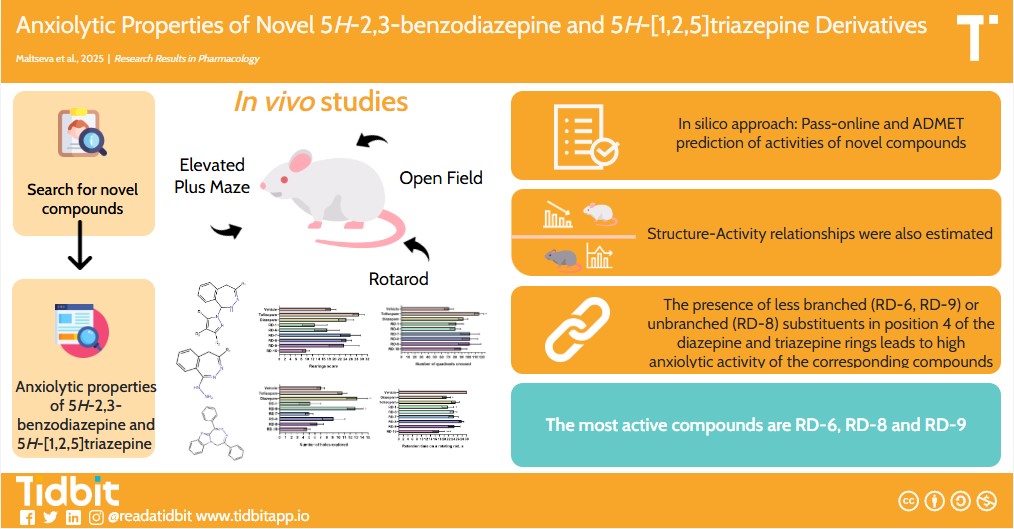
Результаты и обсуждение. При анализе зависимости величины анксиолитического эффекта от строения новых производных 5H-2,3-бензодиазепина и 5H-[1,2,5]триазепина отмечено, что наличие 3,4-диметоксифенильного заместителя в положении 4 диазепинового кольца (RD-1, RD-7) приводит к сниженной анксиолитической активности в сравнении с 4-метоксифенильными производными (RD-6, RD-9). Среди производных 5H-[1,2,5]триазепина более выраженное противотревожное действие оказывало производное с конденсированным бензимидазолом (RD-8) в сравнении с конденсированным пирролом (RD-15). Наличие менее разветвленных (RD-6, RD-9) или не разветвленных (RD-8) заместителей в положении 4 диазепинового и триазепинового колец приводит к высокой анксиолитической активности соответствующих соединений. Соединения не изменяют профиль спонтанной двигательной активности мышей в «Открытом поле». В тесте «Ротарод» отмечено, что отрицательное влияние на мышечный тонус мышей оказывают 4-(3,4-диметоксифенил)-1-гидразино-5H-2,3-бензодиазепин (RD-1) и 4-гидразино-7,8,9-триметил-1-фенил-5H-пирроло[2,1-d][1,2,5]триазепин (RD-15). Согласно ADMET-анализу, соединения RD-6, RD-8 и RD-9 являются малотоксичными, однако рекомендуется исследование специфической токсичности среди данных производных для подтверждения или исключения данных о мутагенности и гепатотоксичности.
Заключение. По совокупности полученных результатов наиболее активным и безопасным для дальнейших исследований соединением среди исследованных производных является 1,4-дифенил-5H-[1,2,5]триазепино[5,4-a]бензимидазол под шифром RD-8.
Графическая аннотация
Ключевые слова:
5H-2,3-бензодиазепин, 5H-[1,2,5]триазепин, ADMET, PASS online, SAR, анксиолитик, открытое полеБиблиографические ссылки
Abu-Hashem AA, Hakami O, Amri N, Mukhrish YE, Abdelgawad AAM (2024) Synthesis of 1,3,5-triazepines and benzo[f][1,3,5]triazepines and their biological activity: recent advances and new approaches. Molecules 29(3): 632. https://doi.org/10.3390/molecules29030632[PubMed] [PMC]
Alwaili MA, Abu-Almakarem AS, Aljohani S, Alkhodair SA, Al-Bazi MM, Eid TM, Alamri J, Mobasher MA, Algarzae NK, A Khayyat AI, Alshaygy LS, El-Said KS (2024) Avenanthramide-C ameliorate doxorubicin-induced hepatotoxicity via modulating Akt/GSK-3β and Wnt-4/β-Catenin pathways in male rats. Frontiers in Molecular Biosciences 11: 1507786. https://doi.org/10.3389/fmolb.2024.1507786 [PubMed] [PMC]
Amaghnouje A, Bohza S, Bohdan N, Es-Safi I, Kyrylchuk A, Achour S, El Fatemi H, Bousta D, Grafov A (2021) New 2,3-benzodiazepine derivative: synthesis, activity on central nervous system, and toxicity study in mice. Pharmaceuticals 14(8): 814. https://doi.org/10.3390/ph14080814 [PubMed] [PMC]
da Silva DM, Sanz G, Vaz BG, de Carvalho FS, Lião LM, de Oliveira DR, da Silva Moreira LK, Cardoso CS, de Brito AF, da Silva DPB, da Rocha FF, Santana IGC, Galdino PM, Costa EA, Menegatti R (2018) Tert-butyl 4-((1-phenyl-1H-pyrazol-4-yl) methyl) piperazine-1-carboxylate (LQFM104) – New piperazine derivative with antianxiety and antidepressant-like effects: Putative role of serotonergic system. Biomedicine & Pharmacotherapy 103: 546–552. https://doi.org/10.1016/j.biopha.2018.04.077 [PubMed]
Daina A, Michielin O, Zoete V (2017) SwissADME: a free web tool to evaluate pharmacokinetics, drug-likeness and medicinal chemistry friendliness of small molecules. Scientific Reports 7(1): 1–13. https://doi.org/10.1038/srep42717 [PubMed] [PMC]
Dong J (2018) ADMETlab: a platform for systematic ADMET evaluation based on a comprehensively collected ADMET database. Journal of Cheminformatics 10(1): 1–11. [PubMed] [PMC]
Groszkowski S, Wrona J (1978) Pyridazino[1,2-a]1,2,5-triazepines. Polish Journal of Pharmacology and Pharmacy 30(5): 713–715. [PubMed]
Khabarov KM, Kharaneko OI, Bogza SL (2009) 2,3-Benzodiazepine-1-thione in the synthesis of substituted and hetero-annelated 2,3-benzodiazepines. Chemistry of Heterocyclic Compounds 45: 468–474.
Kharaneko AO (2017) 7,8,9-trimethyl-1-phenyl-3H-pyrrolo[2,1-d][1,2,5]triazepin-4(5H)-one. Synthesis and reactions. Russian Journal of Organic Chemistry 53(5): 738–745. https://doi.org/10.1134/S1070428017050153
Kharaneko AO (2019) 1,4-Diphenyl-5H-[1,2,5]triazepino[5,4-a]benzimidazole – a new heterocyclic system. Synthesis and Properties. Russian Journal of Organic Chemistry 55(1): 115–117. https://doi.org/0.1134/S1070428019010147
Kraeuter AK, Guest PC, Sarnyai Z (2019) The elevated plus maze test for measuring anxiety-like behavior in rodents. Methods in Molecular Biology 1916: 69–74. https://doi.org/10.1007/978-1-4939-8994-2_4 [PubMed]
Lubrich C, Giesler P, Kipp M (2022) Motor behavioral deficits in the cuprizone model: validity of the rotarod test paradigm. International Journal of Molecular Sciences 23(19): 11342. [PubMed] [PMC]
Nawrocka W, Liszkiewicz H, Wilimowski M, Rutkowska M, Barczyńska J, Kedzierska-Goździk L, Wojewódzki W, Szelag A (1994) Carboxylic esters derivatives of 2-thioxo-1H-2,3,4,5-tetrahydropyrido-[2,3-e]-1,3,4-triazepin-5-ones and 2-thioxo-1H-2,3,4,5-tetrahydro-1,3,4-benzotriazepin-5-ones. Acta Poloniae Pharmaceutica 51(3): 243–248. [PubMed]
Pires DEV, Blundell TL, Ascher DB (2015) pkCSM: predicting small-molecule pharmacokinetic and toxicity properties using graph-based signatures. Journal of Medicinal Chemistry 58(9): 4066–4072. [PubMed] [PMC]
Rudik AV, Dmitriev AV, Lagunin AA, Filimonov DA, Poroikov VV (2019) PASS-based prediction of metabolites detection in biological systems. SAR and QSAR in Environmental Research 30(10): 751–758. https://doi.org/10.1080/1062936X.2019.1665099 [PubMed]
Skripka MO, Spasov AA, Maltsev DV (2021) Screening of anxiolytic properties and analysis of structure-activity relationship of new derivatives of 6-(4-methoxy)-7H-[1,2,4]triazolo[3,4-a][2,3]benzodiazepine under the code RD. Research Results in Pharmacology 7(2): 31–37. https://doi.org/10.3897/rrpharmacology.7.67499
Stefancich G, Massa S, Artico M (1991) Polycyclic diazepine and triazepine derivatives of pharmacological interest. Farmaco 46(1 Suppl): 297–306. [PubMed]
Üçel Uİ, Can ÖD, Demir Özkay Ü, Ulupinar E (2020) Antiamnesic effects of tofisopam against scopolamine-induced cognitive impairments in rats. Pharmacology, Biochemistry, and Behavior 190: 172858. https://doi.org/10.1016/j.pbb.2020.172858 [PubMed]
Yang H, Lou C, Sun L, Li J, Cai Y, Wang Z, Li W, Liu G, Tang Y (2019) AdmetSAR 2.0: web-service for prediction and optimization of chemical ADMET properties. Bioinformatics (Oxford, England) 35(6): 1067–1069. https://doi.org/10.1093/bioinformatics/bty707 [PubMed]
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2025 Maltseva MO, Maltsev DV, Miroshnikov MV, Divaeva LN, Kharaneko AO, Kharaneko OI, Morkovnik AS, Spasov AA

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

