Разработка транскутанной формы дезлоратадина
DOI:
https://doi.org/10.18413/rrpharmacology.10.487Аннотация
Введение: У людей, страдающих аллергией, не всегда есть возможность предотвратить попадание аллергенов в организм. По этой причине важно создать препарат длительного действия, который мог бы предотвратить аллергическую реакцию. Очень перспективным вариантом является трансдермальная терапевтическая система (ТТС) с Н1-блокаторами. Целью исследования было создать технологию производства ТТС на основе дезлоратадина, пригодную для рутинного применения с пролонгированным высвобождением лекарственного средства.
Материалы и методы: В качестве основного полимера-матрицы для TTS использовали поливинилпирролидон К30 (ПВП), а в качестве адгезивного слоя - полимерную мембрану Kruofilm. Формирование полимерной мембраны осуществляли путем высушивания водно-спиртового раствора компонентов при температуре 60ºC. Характеристику полученных лекарственных форм проводили методом спектрофотометрии. Размер полученных мицелл измеряли методом динамического рассеяния света.
Результаты и их обсуждение: Были получены пластыри круглой формы с растворенным в воде дезлоратадином (ДЛ) и его мицеллярной формой. Диаметр пластырей составлял 35 мм, а толщина слоя – 2,5 мм. Размер мицелл с ДЛ составил 22,8 ± 5,2 нм. Был разработан спектрофотометрический метод определения ДЛ. Содержание ДЛ в пластырях варьировалось от 5 до 25 мг на пластырь в зависимости от технологии производства.
Заключение: Нами разработаны ТТС, содержащие ДЛ в виде раствора и мицеллярной формы. Был подобран верхний адгезивный слой, который обладает влагостойкостью, прочностью и надежной фиксацией матрицы с активным веществом на коже. Также был разработан и апробирован метод спектрофотометрического определения ДЛ в растворах и пластырях.
Графическая аннотация
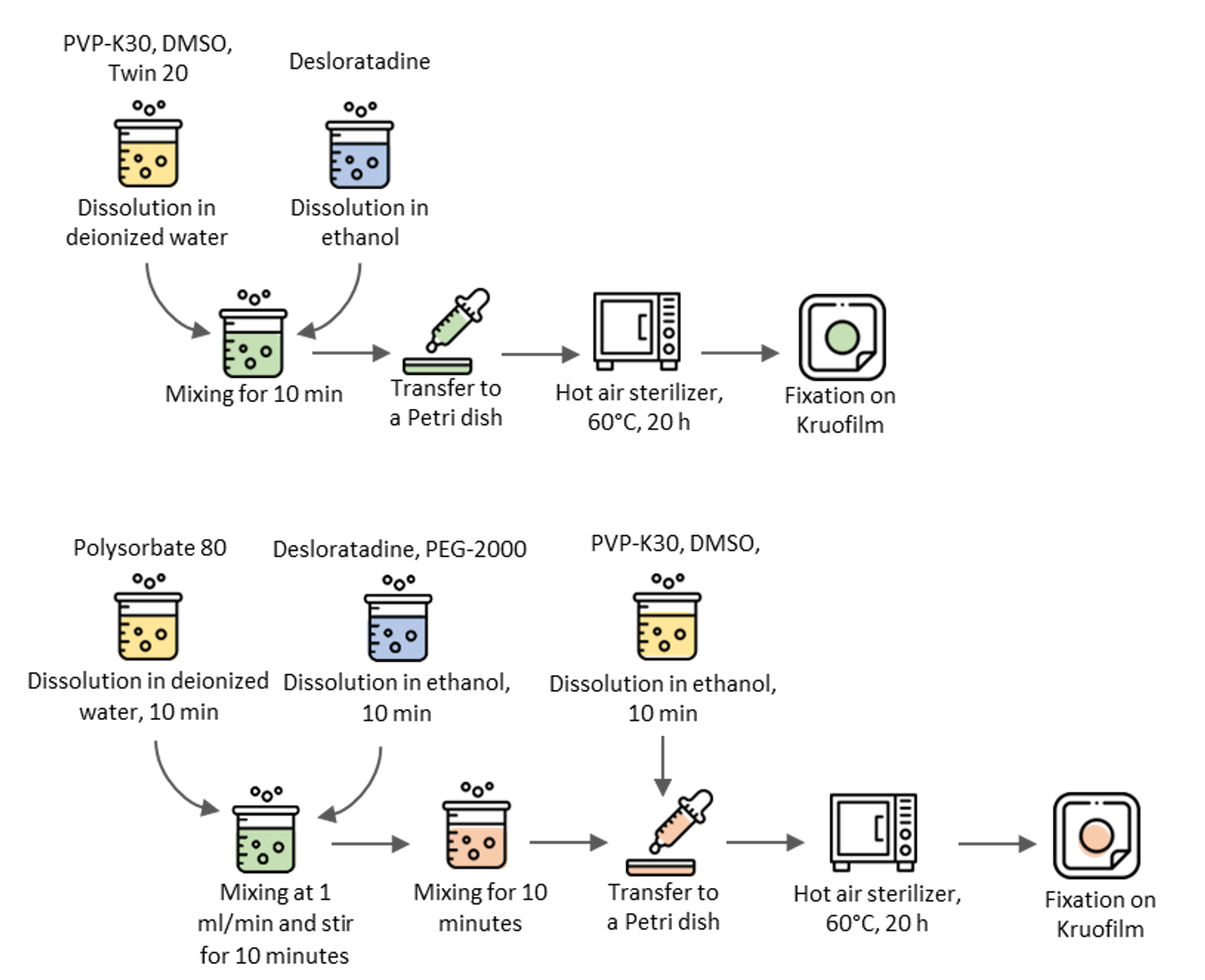
Ключевые слова:
аллергия, дезлоратадин, трансдермальная терапевтическая система, пластыри, мицеллыБиблиографические ссылки
Cheow Chee LEE (2015) Transdermal Drug Delivery Patch: A technology outline. https://doi.org/10.13140/RG.2.1.2929.6162
Devillier P, Roche N, Faisy C (2008) Clinical pharmacokinetics and pharmacodynamics of desloratadine, fexofenadine and levocetirizine: a comparative review. Clinical Pharmacokinetics 47(4): 217–230. https://doi.org/10.2165/00003088-200847040-00001 [PubMed]
Dinesh B, Patil U, Desai B, Raghu K, Sadashivaiah R (2008) Design and in vitro evaluation of haloperidol lactate transdermal patches containing ethyl cellulose-povidone as film formers. Asian Journal of Pharmaceutics 2: 43. https://doi.org/10.4103/0973-8398.41565
Dribin TE, Motosue MS, Campbell RL (2022) Overview of allergy and anaphylaxis. Emergency Medicine Clinics of North America 40(1): 1–17. https://doi.org/10.1016/j.emc.2021.08.007 [PubMed] [PMC]
Fein MN, Fischer DA, O’Keefe AW, Sussman GL (2019) CSACI position statement: newer generation H1-antihistamines are safer than first-generation H1-antihistamines and should be the first-line antihistamines for the treatment of allergic rhinitis and urticaria. Allergy, Asthma & Clinical Immunology 15: 61. https://doi.org/10.1186/s13223-019-0375-9 [PubMed] [PMC]
Gupta R, Mukherjee B (2003) Development and in vitro evaluation of diltiazem hydrochloride transdermal patches based on povidone-ethylcellulose matrices. Drug Development and Industrial Pharmacy 29(1): 1–7. https://doi.org/10.1081/DDC-120016678[PubMed]
Joshi N, Azizi Machekposhti S, Narayan RJ (2023) Evolution of transdermal drug delivery devices and novel microneedle technologies: A historical perspective and review. JID Innovations 3(6): 100225. https://doi.org/10.1016/j.xjidi.2023.100225 [PubMed] [PMC]
Kováčik A, Kopečná M, Vávrová K (2020) Permeation enhancers in transdermal drug delivery: benefits and limitations. Expert Opinion on Drug Delivery 17(2): 145–155. https://doi.org/10.1080/17425247.2020.1713087 [PubMed]
Kulikov OA, Yunina DV, Ageev VP, Shlyapkina VI, Avdyushkina IS, Akmaeva IA, Zaborovsky AV, Tararina LA, Tsaregorodtsev SV, Pyataev NA (2023) Evaluation of cellular toxicity and preclinical safety of using an inhalable liposomal form of dexamethasone. Pharmaceutical Chemistry Journal 56(2): 1573–1576. https://doi.org/10.1007/s11094-023-02829-w [PubMed] [PMC]
Li L, Liu R, Peng C, Chen X, Li J (2022) Pharmacogenomics for the efficacy and side effects of antihistamines. Experimental Dermatology 31(7): 993–1004. https://doi.org/10.1111/exd.14602 [PubMed]
Machekposhti SA, Soltani M, Najafizadeh P, Ebrahimi SA, Chen P (2017) Biocompatible polymer microneedle for topical/dermal delivery of tranexamic acid. Journal of Controlled Release 261: 87–92. https://doi.org/10.1016/j.jconrel.2017.06.016 [PubMed]
Nefodov OO, Belenichev IF, Fedchenko MP, Popazova OO, Ryzhenko VP, Morozova OV (2022) Evaluation of methods of modeling and formation of experimental allergic encephalomyelitis. Research Results in Pharmacology 8(2): 37–48. https://doi.org/10.3897/rrpharmacology.8.77361
Olasińska-Wiśniewska A, Olasiński J, Grajek S (2014) Cardiovascular safety of antihistamines. Advances in Dermatology and Allergology 31(3): 182–186. https://doi.org/10.5114/pdia.2014.43191 [PubMed] [PMC]
Parisi GF, Licari A, Papale M, Manti S, Salpietro C, Marseglia GL, Leonardi S (2020) Antihistamines: ABC for the pediatricians. Pediatric Allergy and Immunology 24: 34–36. https://doi.org/10.1111/pai.13152 [PubMed]
Prausnitz MR, Langer R (2008) Transdermal drug delivery. Nature Biotechnology 26: 1261–1268. https://doi.org/10.1038/nbt.1504 [PubMed] [PMC]
Romualdi P, Santi P, Candeletti S (2017) Alghedon fentanyl transdermal system. Minerva Medica 108(2): 169–175. https://doi.org/10.23736/S0026-4806.16.04930-2
Valeveti SK, Pashikanti S (2023) Design, development, and evaluation of transdermal patches containing memantine hydrochloride. International Journal of Applied Pharmaceutics 15(5): 181–197. https://doi.org/10.22159/ijap.2023v15i5.48481
Warren C, Nimmagadda SR, Gupta R, Levin M (2023) The epidemiology of food allergy in adults. Annals of Allergy, Asthma & Immunology 130(3): 276–287. https://doi.org/10.1016/j.anai.2022.11.026 [PubMed]
Zhang J, Li H, Albakr L, Zhang Y, Lu A, Chen W, Shao T, Zhu L, Yuan H, Yang G, Wheate NJ, Kang L, Wu C (2023) Microneedle-enabled therapeutics delivery and biosensing in clinical trials. Journal of Controlled Release 360: 687–704. https://doi.org/10.1016/j.jconrel.2023.07.023[PubMed]
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2024 Valentin P. Ageev, Andrey V. Zaborovskiy, Dina V. Yunina, Larisa A. Tararina, Mikhail K. Devkota, Dmitry N. Andreev, Aleksandra E. Pyanzina, Vasilisa I. Shlyapkina, Yulia A. Buldygina, Oleg A. Kulikov, Nikolay A. Pyataev

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

