Идентификация и синтез метаболитов 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамида
DOI:
https://doi.org/10.18413/rrpharmacology.10.498Аннотация
Введение: 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамид является новым селективным ингибитором карбоангидразы II типа, обладающим местным действием при инстилляции в глаза. Для проведения полного фармакокинетического исследования данного препарата необходимо обнаружить и синтезировать его метаболиты для оценки их системной экспозиции.
Материалы и методы: Исследование выполнено на 6 крысах линии Wistar и 6 кроликах породы Советская шиншилла. Препарат в виде 1% суспензии вводился по средством внутрибрюшинной инъекции. Отбор проб крови в объёме 0,2 мл осуществлялся в следующие временные точки: до введения и через 1 ч, 2 ч, 4 ч, 24 ч после введения. 150 мкл каждого образца центрифугировали для получения плазмы. У крыс одновременно с помощью метаболических клеток осуществлялся забор мочи: до введения и в интервалы 0-2 ч, 2 - 4 ч, 4-6 ч, 6-24 ч после введения препарата. Идентификация метаболитов в данных объектах проводилась с помощью ВЭЖХ-МС/МС. Затем обнаруженные продукты биотрансформации синтезировались. Подтверждение структуры полученных субстанции выполнено с применением методов ЯМР-спектроскопии и масс-спектрометрии высокого разрешения. На заключительном этапе с помощью ВЭЖХ-МС/МС осуществлялся анализ биологических жидкостей животных и модельных образцов с добавкой синтезированных соединений для установления структуры метаболитов.
Результаты и их обсуждение: Были идентифицированы и синтезированы N-гидрокси-4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамид, 4-(5-(гидроксиметил)-1,3,4-оксадиазол-2-ил)-бензолсульфонамид и 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфоновая кислота. В результате сравнения по времени удерживания, соотношениям площадей хроматографических пиков на основных MRM-переходах, а также масс-спектрам установлено полное совпадение структуры метаболитов и синтезированных веществ.
Заключение: N-гидрокси-4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамид и 4-(5-гидроксиметил-1,3,4-оксадиазол-2-ил)-бензолсульфонамид являются продуктами биотрансформации исследуемого препарата. Установлено, что 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфоновая кислота при разложении N-гидроксиметаболита в пробах мочи в процессе отбора.
Графическая аннотация
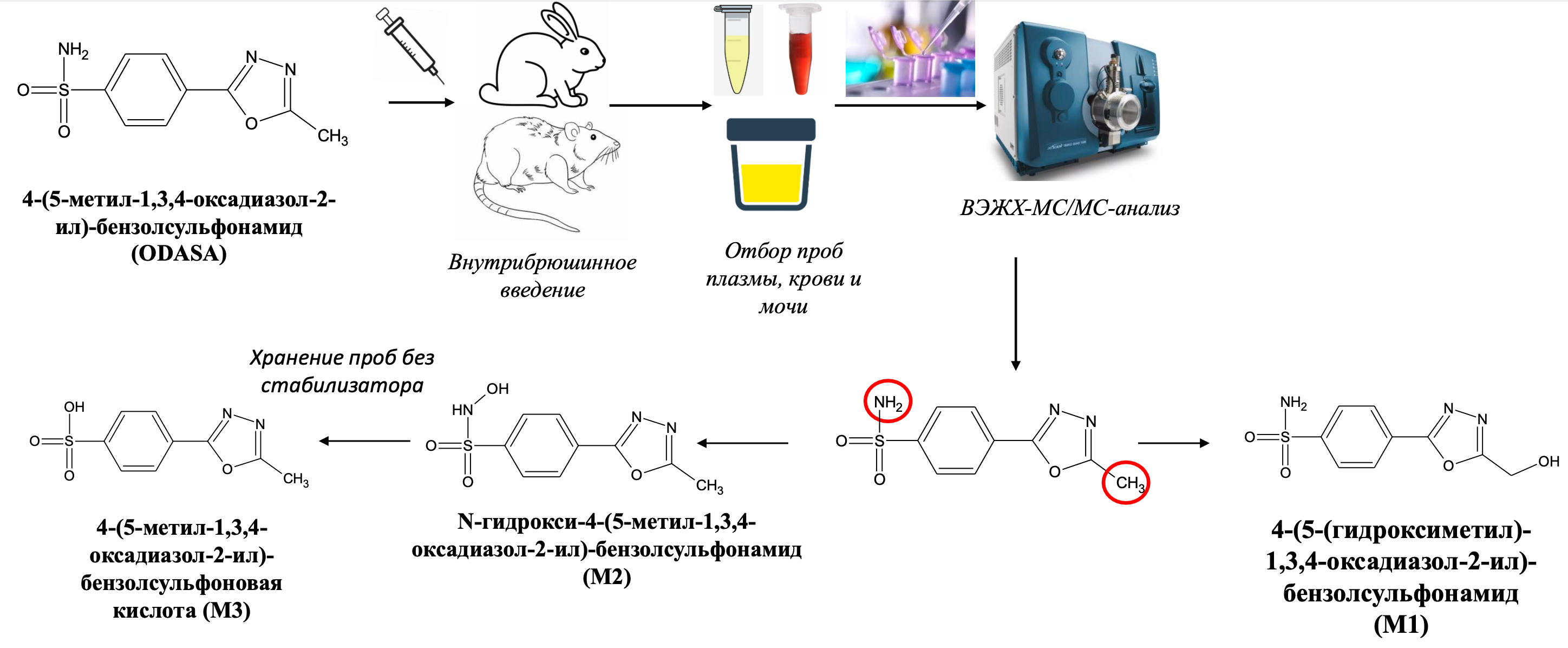
Ключевые слова:
биотрансформация, селективный ингибитор карбоангидразы II, ВЭЖХ-МС/МС, N-гидроксисульфонамидБиблиографические ссылки
Alsibaee AM, Aljohar HI, Attwa MW, Abdelhameed AS, Kadi AA (2023) Investigation of fenebrutinib metabolism and bioactivation using MS3 methodology in ion trap LC/MS. Molecules 28(10): 4225. https://doi.org/10.3390/molecules28104225 [PubMed] [PMC]
Begou O, Drabert K, Theodoridis G, Tsikas D (2020) GC-NICI-MS analysis of acetazolamide and other sulfonamide (R-SO2-NH2) drugs as pentafluorobenzyl derivatives [R-SO2-N(PFB)2] and quantification of pharmacological acetazolamide in human urine. Journal of Pharmaceutical Analysis 10(1): 49–59. https://doi.org/10.1016/j.jpha.2019.11.006[PubMed] [PMC]
Boyce M, Favela KA, Bonzo JA, Chao A, Lizarraga LE, Moody LR, Owens EO,
Patlewicz G, Shah I, Sobus JR, Thomas RS, Williams AJ, Yau A, Wambaugh JF (2023) Identifying xenobiotic metabolites with in silico prediction tools and LCMS
suspect screening analysis. Frontiers in Toxicology 5: 1051483. https://doi.org/10.3389/ftox.2023.1051483 [PubMed] [PMC]
Chen W-H, Chiu C-H, Farn S-S, Cheng K-H, Huang Y-R, Lee S-Y, Fang Y-C, Lin Y-H, Chang K-W (2023) Identification of the hepatic metabolites of flumazenil and their kinetic application in neuroimaging. Pharmaceuticals 16(5): 764. https://doi.org/10.3390/ph1605076 [PubMed] [PMC]
Dhandar AG, Chaudhari SR, Ganorkar SB, Patil AS, Surana SJ (2022) Mini-review on bioanalytical estimation of brinzolamide. Current Pharmaceutical Analysis 18(3): 265–272. https://doi.org/10.2174/1573412917666210812103414
1.2.1.1.0008.15 The Mass-spectrometry» (2023) The State Pharmacopoeia of Russian Federation. XV edition https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/
1.2.1.2.0001.15 The Chromatography (2023) The State Pharmacopoeia of Russian Federation. XV edition https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/
Khokhlov AL, Shetnev AA, Korsakov MK, Fedorov VN, Tyushina AN, Volkhin NN, Vdovichenko VP (2023) Pharmacological properties of sulfonamide derivatives – new inhibitors of carbonic anhydrase. Bulletin of Experimental Biology and Medicine 175(2): 166–170. https://doi.org/10.47056/0365-9615-2023-175-2-166-170 [PubMed]
Khokhlov AL, Yaichkov II, Korsakov MK, Shetnev AA, Volkhin NN, Petukhov SS (2023) Development of quantification methods of a new selective carbonic anhydrase II inhibitor in plasma and blood and study of the pharmacokinetics of its ophthalmic suspension in rats. Research Results in Pharmacology 9(4): 53–64. https://doi.org/10.18413/rrpharmacology.9.10056
Khokhlov AL, Yaichkov II, Shetnev AА, Ivanovsky SA, Korsakov MK, Alexeev MA, Gasilina OA, Volkhin NN, Petukhov SS (2024) Identification and synthesis of metabolites of the new antiglaucoma drug. Research Results in Pharmacology 10(1): 53–66. https://doi.org/10.18413/rrpharmacology.10.431
Kurysheva NI (2020) Carbonic anhydrase inhibitors in the treatment of glaucoma. Review. Part II. Ophthalmology in Russia [Oftal'mologiya] 17(4): 676–682. https://doi.org/10.18008/1816-5095-2020-4-676-682 [in Russian]
Lo Faro AF, Tini A, Gottardi M, Pirani F, Sirignano A, Giorgetti R, Busardò FP (2021) Development and validation of a fast ultra-high-performance liquid chromatography tandem mass spectrometry method for determining carbonic anhydrase inhibitors and their metabolites in urine and hair. Drug Testing and Analysis 13(8): 1552–1560. https://doi.org/10.1002/dta.3055 [PubMed] [PMC]
Peeters L, Vervliet P, Foubert K, Hermans N, Pieters L, Covaci A (2020) A comparative study on the in vitro biotransformation of medicagenic acid using human liver microsomes and S9 fractions. Chemico-Biological Interactions 328: 109192. https://doi.org/10.1016/j.cbi.2020.109192 [PubMed]
Reddy GN, Laltanpuii C, Sonti R (2021) Review on in vivo profiling of drug metabolites with LC-MS/MS in the past decade. Bioanalysis 13(22): 1697–1722. https://doi.org/10.4155/bio-2021-0144 [PubMed]
Simakova IL, Grigoryan LA, Gorbacheva KS (2023) Modern possibilities of functional glaucoma screening (Part 1). National Journal Glaucoma 22(4): 99–111. https://doi.org/10.53432/2078-4104-2023-22-4-99-111 [in Russian]
Trawinski J, Wronski M, Gawlik M, Skibinski R (2022) Identification of the new metabolite of nebivolol using liquid chromatography coupled with high-resolution mass spectrometry and chemometrics. Molecules 27(3): 763. https://doi.org/10.3390/molecules27030763[PubMed] [PMC]
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2024 Khokhlov AL, Yaichkov II, Shetnev AA, Panova VA, Efimova YA, Ivanovskiy SA, Korsakov MK, Vol’khin NN, Petukhov SS

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

