Разработка методик количественного определения в плазме и крови нового селективного ингибитора карбоангидразы II и изучение фармакокинетики его глазной суспензии на крысах
DOI:
https://doi.org/10.18413/rrpharmacology.9.10056Аннотация
Введение: Для изучение системной экспозиции нового селективного ингибитора карбоангидразы II, 4-(2-метил-1,3-оксазол-5-ил)-бензолсульфонамида, и его N-гидроксиметаболита в плазме и в крови необходима разработка новых биоаналитических методик. Результаты эксперимента с однократным введением глазной суспензии изучаемого ЛС необходимы для оптимизации дальнейшего дизайна полного фармакокинетического исследования.
Материалы и методы: Для измерения концентрации аналитов в плазме и крови использовался метод ВЭЖХ-МС/МС. Хроматографическое разделение проводили на колонке Poroshell 120EC-C18 (50*3.0 mm, 2.7 µm). Изучение фармакокинетики проводилось на 6 крысах породы Wistar массой 287,50±18,64 г (M±SD). Каждому животному закапывали по 40 мкл 2% глазной суспензии в каждый глаз. Образцы крови забирали до введения препарата, а также спустя 30 мин, 1 ч, 1ч 30 мин, 2 ч, 3 ч, 4 ч, 6 ч., 8 ч, 12 ч, 24 ч ,48 ч, 72 ч после введения. Некомпартментный подход использовался при расчёте фармакокинетических параметров.
Результаты и обсуждение: Метод осаждения белков выбран для подготовки проб биологических жидкостей. Для предотвращения разложения N-гидросиметаболита препарата к плазме добавлялся 10% раствор аскорбиновой кислоты, а к крови – 10% раствор тиосульфата натрия. Аналитический диапазон определения 4-(2-метил-1,3-оксазол-5-ил)-бензолсульфонамида и его N-гидроксипроизводного в крови составил 50-10000 нг/мл и 5-1000 нг/мл, соответственно, в плазме - 10-2000 нг/мл и 1-200 нг/мл, соответственно. Максимальная концентрация изучаемого препарата в плазме составляет 264,32±68,47 нг/мл (Сред.±SD) через 1,92±0,92 ч (Сред.±SD) после введения, а его метаболита - 10,43±1,79 нг/мл (Сред.±SD) через 2,17±1,13 ч (Сред.±SD) после введения. Величина максимальной концентрации препарата в крови достигает 8705,23±1301,84 нг/мл (Mean±SD) через 1,17±0,52 ч (Mean±SD) после введения, а его N-гидроксиметаболита 230,00±69,54 нг/мл (Mean±SD) через 1,33±0,41 ч (Mean±SD) после введения.
Заключение: Разработанные методики прошли полную валидацию согласно требованиям российских и зарубежных руководств и успешно использованы для фармакокинетического исследования. Установлено, что содержание 4-(2-метил-1,3-оксазол-5-ил)-бензолсульфонамида и его основного метаболита в цельной крови значительно выше, чем в плазме.
Графическая аннотация
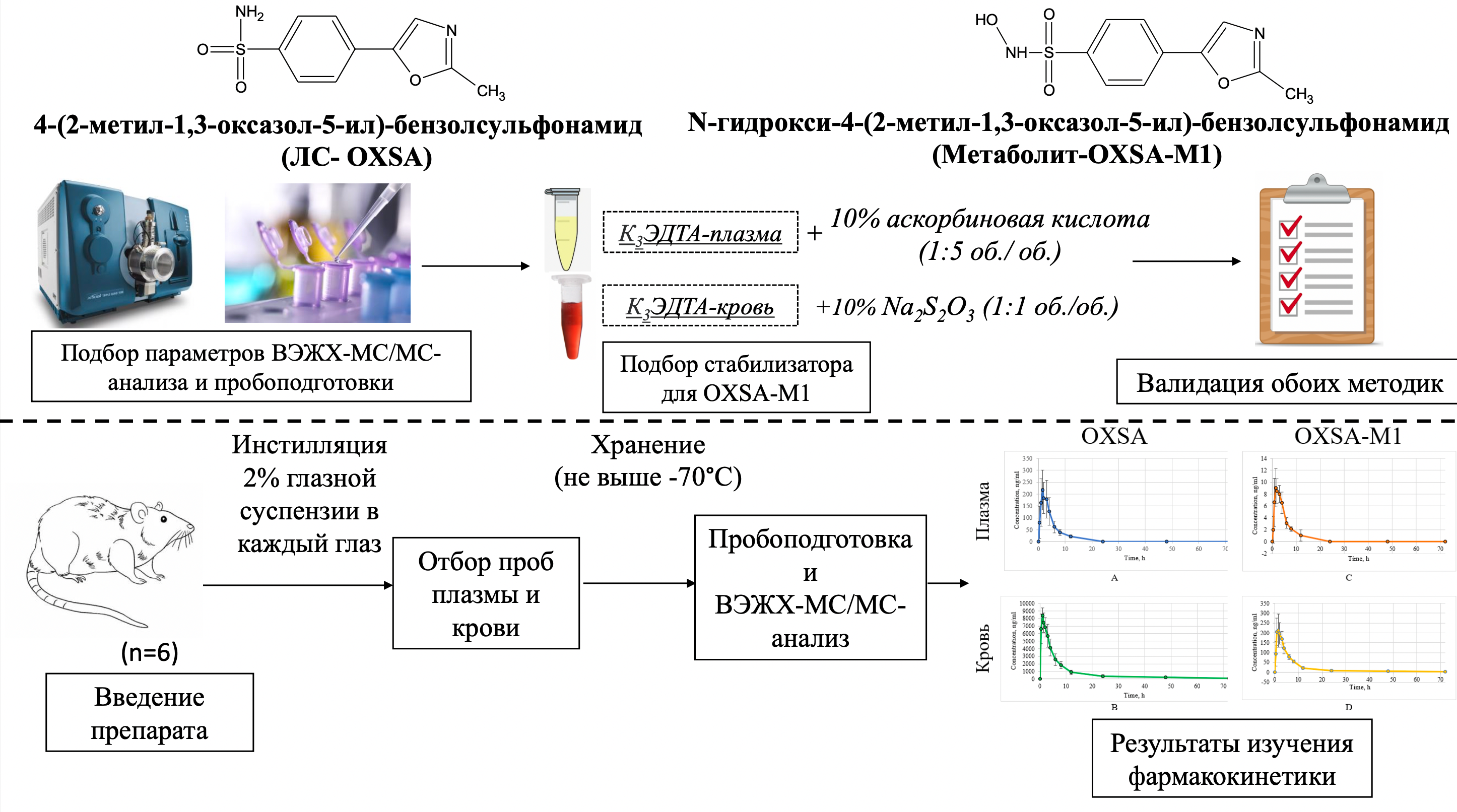
Ключевые слова:
ВЭЖХ-МС/МС, стабилизация, фармакокинетика, селективный ингибитор карбоангидразы IIБиблиографические ссылки
Ferraroni M, Lucarini L, Masini E, Korsakov M, Scozzafava A, Supuran CT, Krasavin M (2017) 1,3-Oxazole-based selective picomolar inhibitors of cytosolic human carbonic anhydrase II alleviate ocular hypertension in rabbits: Potency is supported by X-ray crystallography of two leads. Bioorganic & Medicinal Chemistry 25 (17): 4560–4565. https://doi.prg/10.1016/j.bmc.2017.06.054 [PubMed]
Foivas A, Malenović A, Kostić N, Božić M, Knežević M, Loukas YL, Dotsikas Y (2016) Quantitation of brinzolamide in dried blood spots by a novel LC-QTOF-MS/MS method. Journal of Pharmaceutical and Biomedical Analysis 119(5): 84–90. https://doi.org/10.1016/j.jpba.2015.11.043 [PubMed]
ICH Guideline M10 on Bioanalytical Method Validation and Study Sample Analysis (2022) https://www.ema.europa.eu/en/documents/scientific-guideline/ich-guideline-m10-bioanalytical-method-validation-step-5_en.pdf. (access date: 15 May 2023)
Khokhlov AL, Yaichkov II, Dzhurko YuA, Shitov LN, Shitova AM (2018) Methodical approaches to bioassay of substances containing unstable functional groups. Research Results in Pharmacology 4(1): 33–42. https://doi.org/10.3897/rrpharmacology.4.25253
Kintz P, Gheddar L, Raul J-S (2022) Adverse analytical finding due to red blood cells transfusion: A rare case involving the diuretic dorzolamide. Drug Testing and Analysis 14(10): 1785–1790. https://doi.org/10.1002/dta.3342 [PubMed]
Lo Faro AF, Tini A, Gottardi M, Pirani F, Sirignano A, Giorgetti R, Busardò FP (2021) Development and validation of a fast ultra-high-performance liquid chromatography tandem mass spectrometry method for determining carbonic anhydrase inhibitors and their metabolites in urine and hair. Drug Testing and Analysis 13(8): 1552–1560. https://doi.org/10.1002/dta.3055[PubMed] [PMC]
Madrewar BA, Deshpande A, Bhattacharya S (2022) Mini-Review on bioanalytical estimation of brinzolamide. Current Pharmaceutical Analysis 18(3): 265–272. https://doi.org/10.2174/1573412917666210812103414
Mironov A N (ed.) (2012) Guidelines for Conducting Preclinical Studies of Medicines. Volume 1. Polygraph Plus, Moscow, 944 pp.
Mironov AN (2014) Guidance on Inspection of Medicines. Volume 1. Polygraph Plus, Moscow, 328 рp. [in Russian]
On Approval of the Rules for Conducting Bioequivalence Studies on Medicines in the Eurasian Economic Union. Decision of the Council of the Eurasian Economic Commission №85 of November 3, 2016 (2016) http://docs.cntd.ru/document/456026107 (access date: 15 May 2023).
Strakhov VV, Korsakov MK, Fedorov VN, Vdovichenko VP, Shetnev AA, Popova AA, Volkhin NN (2023) Carbonic anhydrase inhibitors for the treatment of glaucoma. Medical Ethics 1: 44–50. https://doi.org/10.24075/medet.2023.001
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2023 Александр Л. Хохлов, Илья И. Яичков, Михаил К. Корсаков, Антон А. Шетнев, Никита Н. Вольхин, Сергей С. Петухов

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

