Оценка тяжести отсроченных изменений в состоянии нервно-мышечной системы при коррекции местной холодовой травмы III-IV степени препаратом плазмиды pCMV-VEGF165 в эксперименте
DOI:
https://doi.org/10.18413/rrpharmacology.11.550Аннотация
Введение: Спектр клинических проявлений отморожений довольно широк: начиная от травм, которые полностью заживают без каких-либо последствий, до травм, которые приводят к серьезной инвалидизации и ампутации конечностей. Однако даже без значительной потери тканей пациенты могут страдать от долгосрочных последствий после перенесенного отморожения. У 67% пациентов регистрируются долгосрочные осложнения от отморожения, наиболее частыми из них являются невропатия, хроническая боль и функциональные нарушения. Профилактика и лечение долгосрочных осложнений холодовой травмы является важной и сложной задачей.
Исход отморожения зависит от степени микрососудистого повреждения в данной ткани. Использование VEGF (фактора роста эндотелия сосудов) в качестве терапевтического средства при контактной холодовой травме имеет перспективы благодаря его способности стимулировать ангиогенез и улучшать трофику тканей, что может быть критически важно для восстановления поврежденных участков после отморожений.
Цель исследования: изучение эффективности применения генетической конструкции - плазмиды pCMV-VEGF165 при коррекции отсроченных осложнений холодовой травмы у крыс.
Материалы и методы: У 12 половозрелых самок крыс дикого типа массой 275±25 г в соответствии с международными правилами гуманного обращения с лабораторными животными под золетил-ксилазаловым наркозом была смоделирована местная холодовая травма III-IV степени путем контакта охлажденного в жидком азоте (-196°C) неодимового магнита с тыльной поверхностью дистального отдела задней левой конечности в течение 1 минуты. Исследуемый препарат плазмиды pCMV VEGF165 вводился местно на 2 и 7 сутки после моделирования отморожения крысам в края раны в дозе 60 мкг. Крысы контрольной группы получали инъекцию плацебо (вода для инъекций) аналогичным способом. Анализ отсроченных осложнений холодовой травмы был проведен путём оценки состояния нервно-мышечной системы посредством электромиографии на 28 и 60 сутки после моделирования патологии.
Результаты и обсуждение: В группе контроля на 28 сутки эксперимента регистрировалось статистически значимое снижение амплитуда отрицательной фазы М-ответа в 1,86 раза (p=0,004), также статистически достоверно отличавшееся от показателей группы pCMV-VEGF165 (p=0,013). Также выявлено статистически достоверное снижение амплитуды M-ответа в 1,75 (p=0,001) раза. Эти данные свидетельствуют об аксональном повреждении.
Отмечалось статистически достоверное увеличение латентного периода в среднем на 10% от показателей группы интактных животных (p=0,004). Удлинение латентного периода в совокупности с регистрируемыми у ряда животных полифазными ответами и сателлитными потенциалами в группе контроля на 28 сутки эксперимента может косвенно свидетельствовать об имеющейся миелинопатии.
Выраженные изменения отмечались при анализе показателя декремента отрицательной фазы М-ответа: данный показатель статистически достоверно возрастал в группе контроля как на 28, так и на 60 сутки в среднем в 2,2 раза. Рост декремента свидетельствует о развитии нарушения нервно-мышечного проведения в зоне холодовой травмы, что может быть связано со структурными или функциональными изменениями синапса и/или рецепторного аппарата вследствие их повреждения ишемическим, воспалительным или травматическим процессами.
В свою очередь, в группе интактных животных и группе pCMV-VEGF165 показатель амплитуды отрицательной фазы М-ответа был сопоставим, и достигал значений 0,39 [0,35; 0,47] мВ и 0,34±0,08 мВ соответственно (p>0,05). При анализе амплитуды M-ответа выявлено статистически достоверное ее снижение на 28 сутки эксперимента в группе pCMV-VEGF165 в 1,27 раза (p=0,047). Длительность латентного периода в группе pCMV-VEGF165 на 28 сутки также несколько увеличивалась, однако, статистически достоверно от показателей интактных животных не отличалась. Показатель декремента отрицательной фазы М-ответа в группе pCMV-VEGF165 на 28 и 60 сутки не отличался статистически достоверно от группы интактных животных. Отсутствие статистически достоверной разницы по показателю амплитуды отрицательной фазы М-ответа, латентности, декремента в группе pCMV-VEGF165 свидетельствует о способности указанного препарата предупреждать и уменьшать тяжесть повреждения нервных волокон в зоне холодовой травмы.
Заключение: Таким образом, препарат pCMV-VEGF165 благоприятно влияет на развитие отсроченных изменений в состоянии нервно-мышечной системы, что, вероятно, связано с уменьшением степени повреждения тканей и более быстрой их регенерацией вследствие восстановления достаточного уровня кровотока.
Графическая аннотация
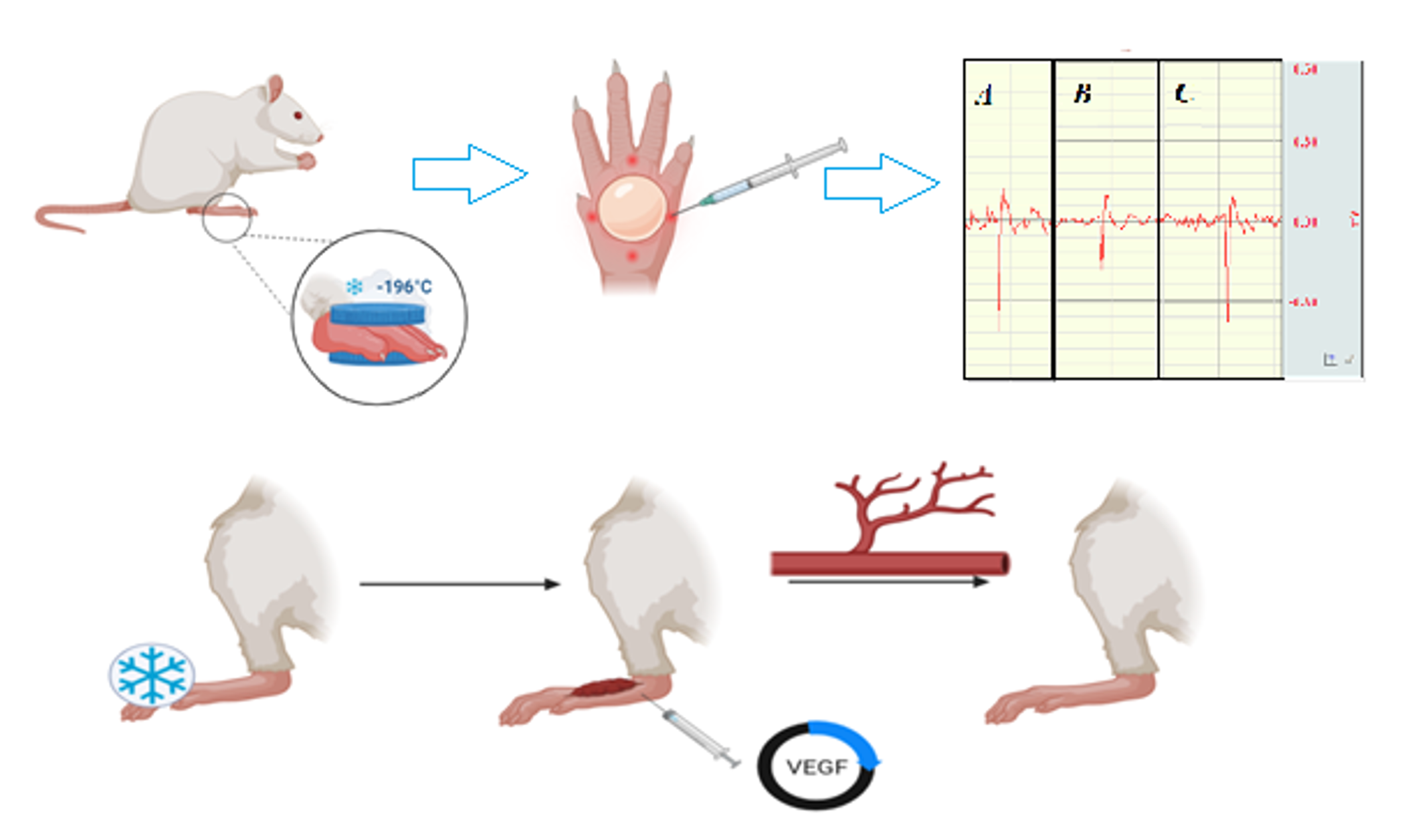
Ключевые слова:
ЭМГ, обморожение, миелинопатия, VEGFБиблиографические ссылки
Aizawa T, Kuwabara M, Kubo S, Aoki S, Azuma R, Kiyosawa T (2019) Protective effect of extract of ginkgo biloba 761 against frostbite injury in rats. Plastic and Reconstructive Surgery 143(6): 1657–1664. https://doi.org/10.1097/PRS.0000000000005648 [PubMed]
Badalyan LO, Skvortsov IA (1986) Clinical Electroneurography: A Guide for Doctors. Medicine, Moscow, 386 pp.
Burleva EP, Babushkina YV (2016) Administration of Neovasculgen agent for treatment of a patient with neuroischaemic form of diabetic foot syndrome. Angiology and Vascular Surgery [Angiologiya i Sosudistaya Khirurgiya] 22(2): 47–51. [in Russian] [PubMed]
Frostbite. Hypothermia. Other effects of low temperature exposure. Clinical recommendations of the Ministry of Health of the Russian Federation (2024) Medical professional non-profit organization “All-Russian public organization Association of Combustiologists “World Without Burns””. URL: https://cr.minzdrav.gov.ru/preview-cr/678_2 (ID: 678_2) [in Russian]
Gorjanc J, Morrison SA, Blagus R, Mekjavic IB (2018) Cold susceptibility of digit stumps resulting from amputation after freezing cold injury in elite alpinists. High Altitude Medicine and Biology 19: 185–192. https://doi.org/10.1089/ham.2017.0134 [PubMed]
Handford C, Thomas O, Imray CHE (2017) Frostbite. Emergency Medicine Clinics of North America 35(2): 281–299. https://doi.org/10.1016/j.emc.2016.12.006 [PubMed]
Imray C, Grieve A, Dhillon S; Caudwell Xtreme Everest Research Group (2009) Cold damage to the extremities: frostbite and non-freezing cold injuries. Postgraduate Medical Journal 85(1007): 481–488. https://doi.org/10.1136/pgmj.2008.068635 [PubMed]
Ishchenko RV, Fistal EYA, Filimonov DA, Pokrovsky MV, Arkhipov BB, Naletov SV, Arefyev BB, Makiyenko BB, Naletova EN (2024) The use of the drug Neovasculgen off-label in the treatment of frostbite of the foot II–III degree: a clinical case. Safety and Risk of Pharmacotherapy [Bezopasnost i Risk Farmakoterapii] 12(4): 409–419. https://doi.org/10.30895/2312-7821-2024-429 [in Russian]
Kapustina E A, Rusanova D V (2007). Electroneuromyographic manifestations in experimental intoxication with vinyl chloride. Acta Biomedica Scientifica (6): 78–80. [in Russian]
McIntosh SE, Freer L, Grissom CK, Auerbach PS, Rodway GW, Cochran A, Giesbrecht GG, McDevitt M, Imray CH, Johnson EL, Pandey P, Dow J, Hackett PH (2019) Wilderness medical society clinical practice guidelines for the prevention and treatment of frostbite: 2019 Update. Wilderness and Environmental Medicine 30(4S): S19–S32. https://doi.org/10.1016/j.wem.2019.05.002 [PubMed]
Murphy JV, Banwell PE, Roberts AH, McGrouther DA (2000) Frostbite: pathogenesis and treatment. The Journal of Trauma 48(1). https://doi.org/10.1097/00005373-200001000-00036 [PubMed]
Pestov YaS (2020) Features of frostbite among soldiers of the Red Army during the Great Patriotic War of 1941-1945. Bulletin of the Northern State Medical University [Byulleten Severnogo Gosudarstvennogo Meditsinskogo Universiteta] 1(44): 10–12. [in Russian]
Regli IB, Strapazzon G, Falla M, Oberhammer R, Brugger H (2021) Long-Term sequelae of frostbite-a scoping review. International Journal f Environmental Research and Public Health 18(18): 9655. https://doi.org/10.3390/ijerph18189655 [PMC] [PubMed]
Shvalb P G, Gavrilenko A V, Kalinin RE, Chervyakov Yu V, Voronov DA, Staroverov INN, Gryaznov S V,Mzhavanadze N, Nersesyan E G, Kiselyov SL, Isaev AA, Deev RV (2011) Efficacy and safety of Neovasculgen in the complex therapy of patients with chronic lower limb ischemia (phase IIb-III clinical trials). Genes and Cells [Geny i Kletki] 6(3): 76–83. [in Russian]
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2025 Darya A. Kostina, Olesya V. Shcheblykina, Anna A. Peresypkina, Vladimir V. Molchanov, Vladimir V. Arkhipov, Nina I. Zhernakova, Valeria S. Simokhina, Chao Zhu, Oleg S. Gudyrev

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

