Идентификация и синтез метаболитов нового производного 4,5-дигидроизоксазол-5-карбоксамида
DOI:
https://doi.org/10.18413/rrpharmacology.10.482Аннотация
Введение: 3-(2-бутил-5-хлоро-1Н-имидазол-4-ил)-N-[4-метокси-3-(трифторметил)фенил]-4,5-дигидро-1,2-оксазол-5-карбоксамид является новым антиревматоидным препаратом. Для полного фармакокинетического исследования данного препарата необходимо идентифицировать и синтезировать продукты его биотрансформации.
Материалы и методы: Исследование биотрансформации проводилось путём внутрибрюшинного введения лекарственного препарата крысам линии Wistar и кроликам породы Советская шиншилла. У животных отбирали образцы крови до введения и через 0,5 ч, 1 ч, 2 ч, 4 ч, 24 ч после введения изучаемого соединения. Данные образцы немедленно центрифугировали для получения плазмы. Моча одновременно отбиралась у крыс до введения и в промежутки 0-2 ч, 2 - 4 ч, 4-6 ч, 6-24 ч после введения; фекалии - до введения и в промежутки 0-12 ч и 12-24 ч после введения. После немедленной пробоподготовки путём добавления ацетонитрила образцы анализировали с помощью ВЭЖХ-МС/МС.
Результаты: 3-(2-бутил-5-хлоро-1Н-имидазол-4-ил)-4,5-дигидро-1,2-оксазол-5-карбоновая кислота и 4-метокси-3-(трифторметил)анилин - продукты гидролиза действующего вещества были обнаружены в ходе анализа проб плазмы, мочи и фекалий. Производное 4,5-дигидро-1,2-оксазол-5-карбоновой кислоты было синтезировано. Второй метаболит является сырьём для получения активной фармацевтической субстанции. В ходе сравнительных испытаний было установлено отсутствие значимых различий во времени удерживания, соотношении площадей хроматографических пиков на основных MRM-переходах и масс-спектрах этих метаболитов на хроматограммах стандартных образцов и образцов животных. Это свидетельствует о правильной идентификации продуктов биотрансформации.
Выводы: Изучаемый препарат подвергается биотрансформации путём гидролиза с образованием двух основных метаболитов: 3-(2-бутил-5-хлоро-1Н-имидазол-4-ил)-4,5-дигидро-1,2-оксазол-5-карбоновой кислоты и 4-метокси-3-(трифторметил)аналина. Структура метаболитов подтверждена путём сравнения с синтезированными стандартными образцами с помощью ВЭЖХ-МС/МС.
Графическая аннотация
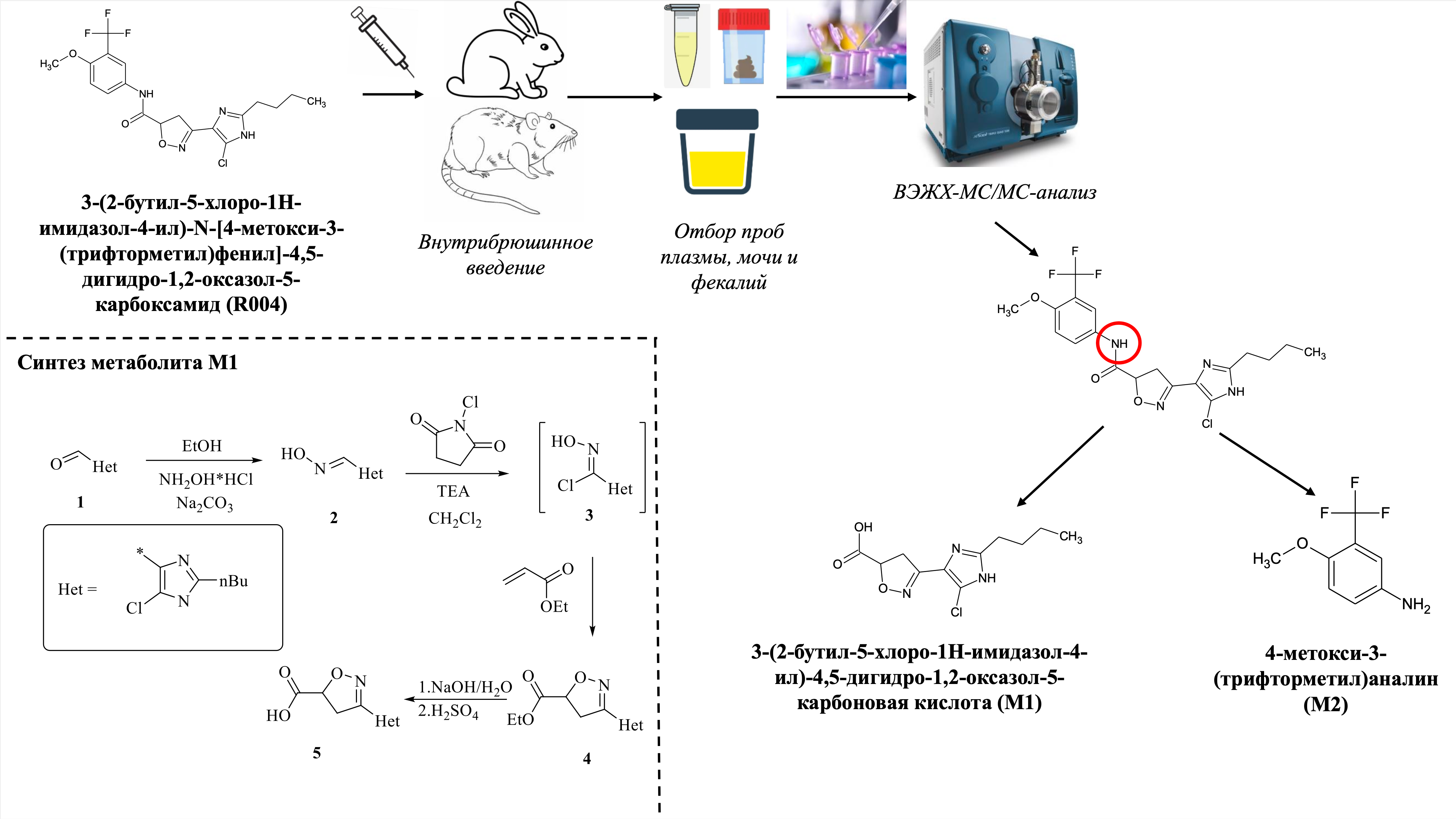
Ключевые слова:
производное 4,5-дигидроизоксазол-5-карбоксамида, биотрансформация, ингибитор PAR-2, ВЭЖХ-МС/МС, гидролизБиблиографические ссылки
Alseekh S , Aharoni A, Brotman Y, Contrepois K, D’Auria J, Ewald J (2021) Mass spectrometry-based metabolomics: a guide for annotation, quantification and best reporting practices. Nature Methods 18(7): 747–756. https://doi.org/10.1038/s41592-021-01197-1
Begou O, Drabert K, Theodoridis G, Tsikas D (2020) GC-NICI-MS analysis of acetazolamide and other sulfonamide (R-SO2-NH2) drugs as pentafluorobenzyl derivatives [R-SO2-N(PFB)2] and quantification of pharmacological acetazolamide in human urine. Journal of Pharmaceutical Analysis 10(1): 49–59. https://doi.org/10.1016/j.jpha.2019.11.006
Dhandar AG, Chaudhari SR, Ganorkar SB, Patil AS, Surana SJ (2022) Mini-review on bioanalytical estimation of brinzolamide. Current Pharmaceutical Analysis 18(3): 265–272. https://doi.org/10.2174/1573412917666210812103414
Ferraroni M, Lucarini L, Masini E, Korsakov M, Scozzafava A, Supuran CT, Krasavin M (2017) 1,3-Oxazole-based selective picomolar inhibitors of cytosolic human carbonic anhydrase II alleviate ocular hypertension in rabbits: Potency is supported by X-ray crystallography of two leads. Bioorganic & Medicinal Chemistry 25 (17): 4560–4565. https://doi.prg/10.1016/j.bmc.2017.06.054 [PubMed]
1.2.1.1.0008.15 «The mass-spectrometry» (2023) The State Pharmacopoeia of Russian Federation. XV edition https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/
1.2.1.2.0001.15 «The Chromatography» (2023) The State Pharmacopoeia of Russian Federation. XV edition https://pharmacopoeia.regmed.ru/pharmacopoeia/izdanie-15/
Khokhlov AL (ed.), Pyatigorskaya NV (ed.) (2019) Industrial Pharmacy: The Way to Create a Product. The Russian Scientific Academy, Moscow, 394 pр. ISBN: 978-5-907036-57-4.
Khokhlov AL, Shetnev AA, Korsakov MK, Fedorov VN, Tyushina AN, Volkhin NN, Vdovichenko VP (2023) Pharmacological properties of sulfonamide derivatives – new inhibitors of carbonic anhydrase. Bulletin of Experimental Biology and Medicine 175 (2): 166–170. https://doi.org/10.47056/0365-9615-2023-175-2-166-170
Khokhlov AL, Yaichkov II, Korsakov MK, Shetnev AA, Volkhin NN, Petukhov SS (2023) Development of quantification methods of a new selective carbonic anhydrase II inhibitor in plasma and blood and study of the pharmacokinetics of its ophthalmic suspension in rats. Research Results in Pharmacology 9(4): 53–64. https://doi.org/10.18413/rrpharmacology.9.10056
Lo Faro AF, Tini A, Gottardi M, Pirani F, Sirignano A, Giorgetti R, Busardò FP (2021) Development and validation of a fast ultra-high-performance liquid chromatography tandem mass spectrometry method for determining carbonic anhydrase inhibitors and their metabolites in urine and hair. Drug Testing and Analysis 13(8): 1552–1560. https://doi.org/10.1002/dta.3055 [PubMed] [PMC]
Ma Y, Modrzynski JJ, Yang Y, Aamand J, Zheng Y (2021) Redox-dependent biotransformation of sulfonamide antibiotics exceeds sorption and mineralization: Evidence from incubation of sediments from a reclaimed water-affected river. Water Research 205: 117616. https://doi.org/10.1016/j.watres.2021.117616
Mironov AN (ed.) (2012) Guidelines for Conducting Preclinical Studies of Medicines. Volume 1. Polygraph Plus, Moscow, 944 pp.
Reddy GN, Laltanpuii C, Sonti R (2021) Review on in vivo profiling of drug metabolites with LC-MS/MS in the past decade. Bioanalysis 13(22): 1697–1722. https://doi.org/10.4155/bio-2021-0144
Sibinčić N, Kalinin S, Sharoyko V, Efimova J, Gasilina OA, Korsakov M et al (2023) A series of trifluoromethylisoxazolyl- and trifluoromethylpyrazolyl-substituted (Hetero) aromatic sulfonamide carbonic anhydrase inhibitors: Synthesis, and convenient prioritization workflow for further in vivo studies. Medicinal Chemistry 19(2): 193–210. https://doi.org/10.2174/1573406418666220831112049
Vree TB, Hekster YA, Tijhuis MW (1985) Metabolism of sulfonamides. Antibiotics and Chemotherapy. Pharmacokinetics of Sulfonamides Revisited 34: 5–65. https://doi.org/https://doi.org/10.1159/000410271
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2024 Alexander L. Khokhlov, Ilya I. Yaichkov, Mikhail K. Korsakov, Anton A. Shetnev, Sergey A. Ivanovskiy, Mikhail A. Alexeev, Olga A. Gasilina, Nikita N. Volkhin, Sergey S. Petukhov

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

