Оценка фармакокинетических параметров 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамида и его метаболитов в плазме крови крысы
DOI:
https://doi.org/10.18413/rrpharmacology.10.523Аннотация
Актуальность: 4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамид (ODASA) - новое фармакологически активное соединение, способное снижать внутриглазное давление за счёт ингибирования карбоангидразы II типа. В рамках доклинического исследования необходимо рассчитать фармакокинетические параметры данного соединения и его метаболитов в плазме крови лабораторных животных.
Цель: Оценка фармакокинетических параметров ODASA и его метаболитов в плазме крови крысы после инстилляции глазной суспензии и её внутрибрюшинного введения.
Материалы и методы: Исследование проводилось на 2 группах крыс линии Wistar по 6 особей. Первой группе проводили инстилляцию 1% глазной суспензии ODASA по 20 мкл в каждый глаз (1,6 мг/кг). Второй группе препарат вводили внутрибрюшинно в той же дозе. Отбор проб крови проводили до введения, через 0,5, 1 ч, 2 ч, 4 ч, 6 ч, 8 ч, 12 ч, 24 ч, 48, ч, 72 ч, 96 ч, 120 ч, 144 ч, 192 ч, 240 ч, 288 ч после введения. Плазму немедленно стабилизировали 10% раствором аскорбиновой кислоты и замораживали до температуры не выше -70°С. Анализ образцов проводили методом ВЭЖХ-МС/МС. Хроматографическое разделение проводили на колонке Kinetex Phenyl Hexyl (50*4.6 мм, 2.6 мкм) в градиентном режиме. Детектирование осуществлялось в режиме MRM с применением электрораспылительной ионизации
Результаты: Разработанная методика валидирована в диапазоне 2-2000 нг/мл для ODASA и 4-[5-(гидроксиметил)-1,3,4-оксадиазол-2-ил]-бензолсульфонамида (М1) и 0,5 -500,0 нг/мл для N-гидрокси-4-(5-метил-1,3,4-оксадиазол-2-ил)-бензолсульфонамида (М2). Величина максимальной концентрации в плазме после закапывания в глаза у ODASA составила 349.85±62.50 нг/мл, у М1 – 30,91±6,00 нг/мл, у М2 – 2,70±0,62 нг/мл (M±SEM). Период полувыведения ODASA после инстилляции в глаза составил 46,4±3,8 ч, М1 – 70,0±14.3 ч, М2 – 36,5±15,2 ч (M±SEM). Относительная биодоступность по сравнению с инъекцией составила 81,03%.
Выводы: Выполненная валидация разработанной методики гарантировала достоверность полученных результатов Действующее вещество имеет высокую относительную биодоступность после инстилляции в глаза. М1 является основным метаболитом, а М2 -минорным метаболитом. У изучаемых соединений наблюдался длительный период полувыведения.
Графическая аннотация
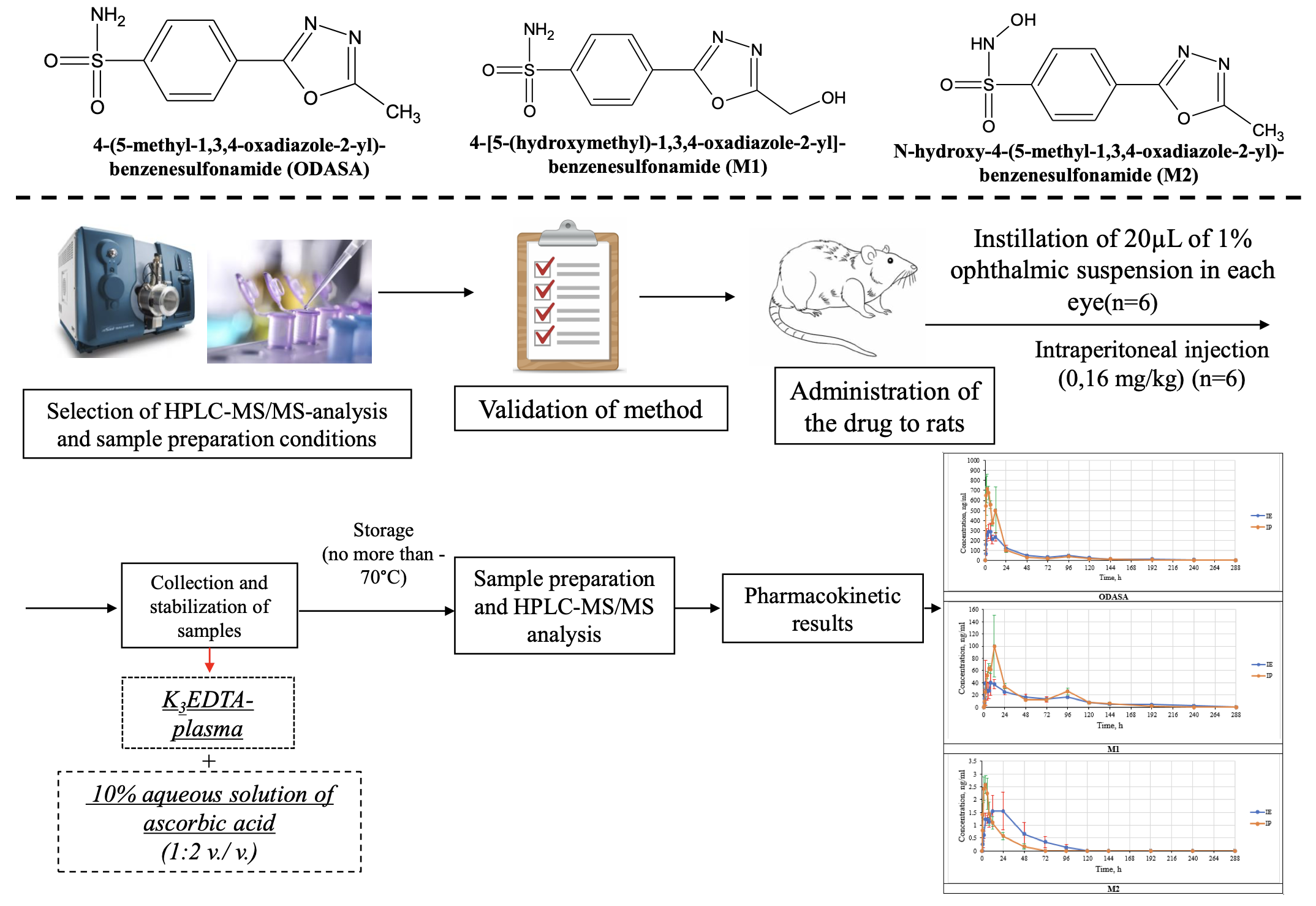
Ключевые слова:
ВЭЖХ-МС/МС, плазма, стабилизация, валидация, фармакокинетика, биодоступность, крысы, ингибитор карбоангидразы II, N-гидроксисульфонамидБиблиографические ссылки
Begou O, Drabert K, Theodoridis G, Tsikas D (2020) GC-NICI-MS analysis of acetazolamide and other sulfonamide (R-SO2-NH2) drugs as pentafluorobenzyl derivatives [R-SO2-N(PFB)2] and quantification of pharmacological acetazolamide in human urine. Journal of Pharmaceutical Analysis 10(1): 49–59. https://doi.org/10.1016/j.jpha.2019.11.006[PubMed] [PMC]
Dhandar AG, Chaudhari SR, Ganorkar SB, Patil AS, Surana SJ (2022) Mini-review on bioanalytical estimation of brinzolamide. Current Pharmaceutical Analysis 18(3): 265–272. https://doi.org/10.2174/1573412917666210812103414
ICH guideline M10 on bioanalytical method validation and study sample analysis (2022) https://www.ema.europa.eu/en/documents/scientific-guideline/ich-guideline-m10-bioanalytical-method-validation-step-5_en.pdf. (access date: 16.08.2024)
Khokhlov AL, Yaichkov II, Korsakov MK, Shetnev AA, Volkhin NN, Petukhov SS (2023) Development of quantification methods of a new selective carbonic anhydrase II inhibitor in plasma and blood and study of the pharmacokinetics of its ophthalmic suspension in rats. Research Results in Pharmacology 9(4): 53–64. https://doi.org/10.18413/rrpharmacology.9.10056
Khokhlov AL, Yaichkov II, Panova VA, Efimova YA, Shetnev AА, Ivanovsky SA, Korsakov MK, Volkhin NN, Petukhov SS (2024) Identification and synthesis of metabolites of 4-(5-methyl-1,3,4-oxadiazole-2-yl)-benzenesulfonamide. Research Results in Pharmacology 10(4): 15–27. https://doi.org/10.18413/rrpharmacology.10.498
Lo Faro AF, Tini A, Gottardi M, Pirani F, Sirignano A, Giorgetti R, Busardò FP (2021) Development and validation of a fast ultra-high-performance liquid chromatography tandem mass spectrometry method for determining carbonic anhydrase inhibitors and their metabolites in urine and hair. Drug Testing and Analysis 13(8): 1552–1560. https://doi.org/10.1002/dta.3055 [PubMed] [PMC]
Malygin AS, Popov NS, Demidova MA, Shatokhina NA (2020) Development and validation of HPLC-MS/MS method of determination of a new derivative of valproleic acid and 1,3,4-thiadiazole in rabbit blood plasma for pharmacokinetic study. Problems of Biological, Medical, and Pharmaceutical Chemistry [Voprosy Biologhicheskoi, Meditsinskoi i Farmatsevticheskoi Khimii] 23(8): 26–33. https://doi.org/10.29296/25877313-2020-08-04 [in Russian]
Mironov AN (ed.) (2012) Guidelines for Conducting Preclinical Studies of Medicines. Volume 1. Polygraph Plus, Moscow, 944 pp.
On Approval of the Rules for Conducting Bioequivalence Studies on Medicines in the Eurasian Economic Union. Decision of the Council of the Eurasian Economic Commission № 85 of November 3 (2016) http://docs.cntd.ru/document/456026107 (access date: 16.08.2024).
Xiong J, Xu Y, He S, Zhang Y, Wang Z, Wang S, Jiang H (2020) Pharmacokinetics and bioavailability of tildipirosin in rabbits following single-dose intravenous and intramuscular administration. Journal of Veterinary Pharmacology and Therapeutics. 43(5): 448–453. https://doi.org/10.1111/jvp.12882 [PubMed]
Yaichkov II, Korsakov MK, Shetnev AA, Volkhin NN, Petukhov SS (2024) Development and validation of the method of quantification of 5-[5-(trifluoromethyl)-1,2-oxazole-3-yl]-furan-2-sulfonamide and its metabolites in laboratory animal plasma. Drug Development & Registration [Razrabotka i Registratsiya Lekarstvennykh Sredstv] 13(3): 219–230. https://doi.org/10.33380/2305-2066-2024-13-3-1771 [in Russian]
Wilson S E, Carpenter J W, Gardhouse S, KuKanich B (2023) Pharmacokinetics of mavacoxib in New Zealand White rabbits (Oryctolagus cuniculus). American Journal of Veterinary Research. 84 (5): 1–5. https://doi.org/10.2460/ajvr.22.11.0196 [PubMed]
Загрузки
Опубликован
Как цитировать
Выпуск
Раздел
Лицензия
Copyright (c) 2024 Khokhlov AL, Yaichkov II, Shetnev AA, Korsakov MK, Volkhin NN, Petukhov SS, Tyushina AN, Lasaryanz OE

Это произведение доступно по лицензии Creative Commons «Attribution» («Атрибуция») 4.0 Всемирная.
 Русский
Русский
 English
English

